随着抗生素耐药性问题日益严峻,噬菌体因其高度特异性的宿主识别能力而成为精准抗菌策略的重要候选。噬菌体通过识别宿主细胞表面受体启动感染。其中尾尖蛋白的受体结合结构域(receptor binding domain,RBD)所介导的精准识别,是决定其宿主范围与感染效率的关键。此前,王佳伟课题组已在分子层面解析了λ噬菌体识别细菌受体并触发感染的结构机制。然而当受体类型发生改变时,这一识别与激活路径是否在同类噬菌体中保持保守性?以及是否可以基于结构信息实现对噬菌体受体识别特异性的理性设计与调控?这些问题仍有待系统阐明。
2026年2月27日,清华大学生命科学学院/北京生物结构前沿研究中心王佳伟课题组围绕λ样(λ-like)噬菌体A8展开系统研究,在《Structure》发表题为“Structures of lambda-like phage A8 tail tip bound to OmpC provide insight into receptor recognition”的研究论文。该研究解析了A8尾尖蛋白gpJ截断体(gpJ713)在未结合态及受体结合态下的高分辨率冷冻电镜结构,揭示了受体识别诱导的构象级联变化机制,并验证了结构引导的受体编程可行性。
一.解析A8尾尖蛋白两种状态下的结构
研究团队利用冷冻电镜技术,解析了A8 gpJ713(3.49 Å)及A8 gpJ713与宿主外膜蛋白OmpC结合(3.84 Å)下的结构(图1)。结构分析显示,当A8 gpJ713与OmpC结合后,远端RBD结构域深入OmpC的中央孔道,触发了RBD刚体运动,进一步驱动了CSF结构域中β1和β2链的位移,使其与β3链形成稳定的氢键,启动信号向上传递,最终诱导AHS结构域发生约180°的翻转,折叠至CSF结构之上引发感染。这一结果表明,受体结合并非简单的局部界面接触,而是一个协同的整体构象级联过程。
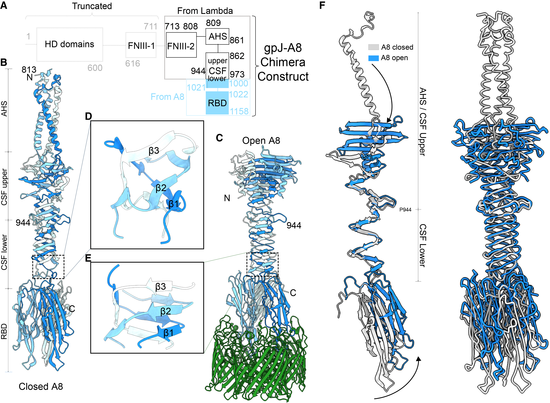
图1. A8 gpJ713结合受体OmpC前后的结构
二.揭示构象激活路径的保守性
通过将A8-OmpC复合物与王佳伟课题组此前解析的经典λ-LamB复合物进行深度比对发现,尽管两者识别的受体(OmpC和LamB)几何形状迥异,但其尾尖蛋白内部的构象激活路径具有高度一致性。这一发现确立了λ样噬菌体共享的通用机械框架:即通过远端受体驱动RBD旋转位移,触发CSF结构域的机械开关,进而向上游传导感染信号。
三.结构预测指导受体识别调控与编程
基于该结构模型,研究团队探索了理性重塑噬菌体宿主范围的可能性。根据结构推测天然变体OmpC G40因胞外环EL4的插入导致与A8 RBD产生空间位阻,从而产生感染抗性。团队通过精准删除该插入片段,成功恢复了高亲和力结合。团队进一步挑战了原本无法被λ噬菌体识别的受体OmpF。结构预测显示,OmpF的EL6环区过长构成了主要位阻。通过将该环进行截断,研究团队成功将OmpF转变为功能性受体,实现了受体特异性的跨越(图2)。
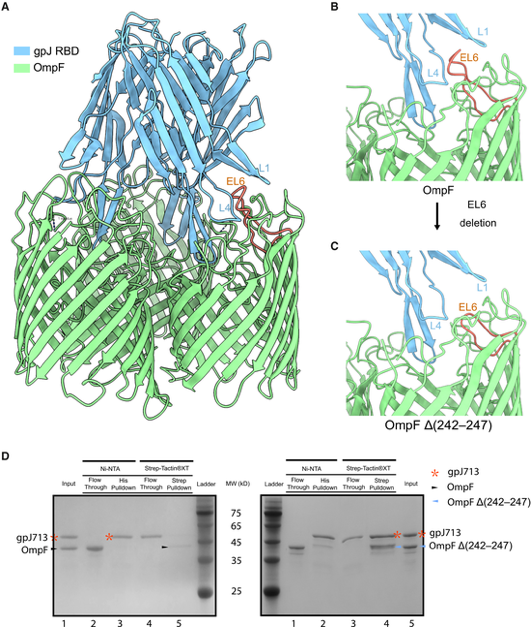
图2. 重新编程OmpF使其结合λ RBD
四. 为可编程噬菌体疗法提供理论基础
在抗生素耐药问题日益严峻的背景下,工程化改造噬菌体以精准控制其宿主范围具有重要临床价值。本研究不仅揭示了噬菌体感染启动的分子细节,更证明了基于高分辨率结构的理性设计可以绕过漫长的定向进化,实现受体识别的精准重编程。
清华大学生命科学学院/北京生物结构前沿研究中心王佳伟副教授和清华大学生命科学学院博士毕业生葛霄飞为本文共同通讯作者。清华大学生命科学学院25届博士毕业生邓婷月为本文第一作者。该研究得到了国家自然科学基金等项目的支持。
王佳伟课题组相关研究列表
Wang C, Zeng J, Wang J. Structural basis of bacteriophage lambda capsid maturation. Structure. 2022 Apr 7;30(4):637-645.e3. doi: 10.1016/j.str.2021.12.009. Epub 2022 Jan 12. PMID: 35026161.
Wang C, Duan J, Gu Z, Ge X, Zeng J, Wang J. Architecture of the bacteriophage lambda tail. Structure. 2024 Jan 4;32(1):35-46.e3. doi: 10.1016/j.str.2023.10.006. Epub 2023 Nov 1. PMID: 37918400.
Gu Z, Wu K, Wang J. Structural morphing in the viral portal vertex of bacteriophage lambda. J Virol. 2024 May 14;98(5):e0006824. doi: 10.1128/jvi.00068-24. Epub 2024 Apr 25. PMID: 38661364; PMCID: PMC11092355.
Ge X, Wang J. Structural mechanism of bacteriophage lambda tail's interaction with the bacterial receptor. Nat Commun. 2024 May 17;15(1):4185. doi: 10.1038/s41467-024-48686-3. PMID: 38760367; PMCID: PMC11101478.
Gu, Z., Ge, X. & Wang, J. Structure of an F-type phage tail-like bacteriocin from Listeria monocytogenes. Nat Commun 16, 1695 (2025). https://doi.org/10.1038/s41467-025-57075-3









