在革兰阴性细菌中,外膜是抵御抗菌物质和免疫攻击的第一道防线,而外膜蛋白的插入依赖β-桶组装机器(BAM)。在大肠杆菌中,BAM复合物由BamA和四个脂蛋白亚基组成,其中BamA和BamD是必需组分。BamA具有16股β-桶结构和五个POTRA结构域,可与底物形成“混合桶”以促进蛋白折叠。相比之下,Bacteroidota(拟杆菌)门细菌的外膜蛋白更大、结构更复杂,并含有大量表面脂蛋白。以往研究推测其BAM系统可能功能扩展,不仅插入OMP,还参与SLP的定位及SUS系统的组装。此外,Bacteroidota的BAM复合物可能与特有的9型分泌系统(T9SS)功能相关。为此,来自牛津大学的SusanM. Lea和Ben C. Berks团队从来源于Bacteroidota门细菌,T9SS-阳性的Flavobacteriumjohnsoniae中分离并解析了该类BAM复合物。

研究者通过在BamA上融合亲和标签,成功纯化并解析了F.johnsoniae 的BAM复合物(BAMFj)。该复合物除BamA外含有五个亚基:BamD、BamG、BamH、BamM和BamP,其中BamG、BamH、BamM和BamP均为新发现的组分(图 1a、b)。与E.coli中所有辅助亚基均位于周质不同,BAMFj 的结构高度重塑(图1):BamG为跨膜外膜蛋白,BamH和BamM为表面脂蛋白,共同形成一个覆盖在BamA上的“伞状”胞外结构,而BamD和BamP位于周质侧(图 1b,c)。BamG属于FadL家族,其β-桶结构通过脂质和糖基化修饰稳定,并与BamA紧密相互作用。BamH–BamM复合物沿轴线相互嵌合,形成一个疏水沟槽状表面,覆盖在底物蛋白折叠区域上方。总体来看,BAMFj通过独特的胞外伞状结构与多层脂质-蛋白相互作用,为Bacteroidota门复杂外膜蛋白的组装提供了结构基础。
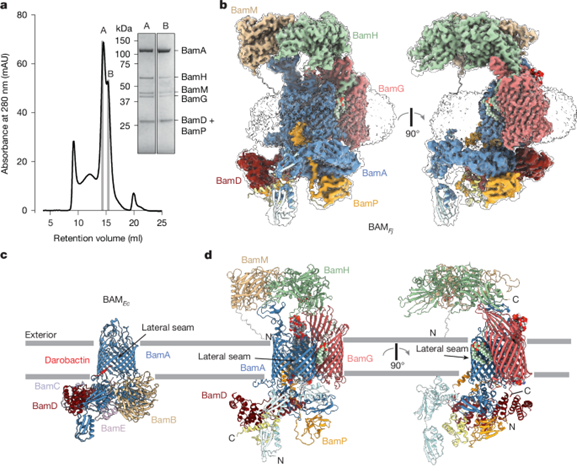
图1. BAMFj复合物的结构
在BAMFj 复合物中,BamP 的中心环结构嵌入BamA 的侧缝,阻碍了底物形成杂合桶结构,因此该状态可能代表不活跃或抑制态。删除BamP 后,BamA 复合物失去了部分辅助亚基,仅形成BamAD 复合物,且 BamA 桶的侧缝仍为关闭状态(图 2)。该结构类似 E.coli BAM 与底物结合的末端插入状态,提示 BamP 缺失可能模拟OMP 插入后的构象。BamP的环结构占据了 darobactin 的结合位点,使拟杆菌门对该抗生素天然耐受。删除BamP 同源物会使细菌对 darobactin 敏感,而过表达BamP 可恢复耐受性。
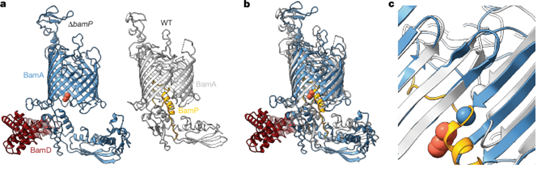
图2. BamP缺失的结构
为探究必需蛋白 BamG 和BamH 的功能,研究人员建立了一个可控基因耗竭系统,通过TetR调控启动子在 F.johnsoniae 中实现对 BamA、BamG和 BamH 的逐步耗竭。结果表明,这三种蛋白都是细胞生长所必需的,其耗竭会导致外膜(OM)严重畸形、囊泡生成停止、并出现明显的胞质外泄(图 3a)。免疫印迹分析显示,BamA、BamG或 BamH 耗竭均会显著降低多种外膜蛋白(OMP)与表面脂蛋白(SLP)的水平(图 3b),说明它们对外膜蛋白生物合成至关重要。该现象并非源于囊泡释放增加,而是由于OMP插入缺陷所致。此外,降低 BamH 的稳定表达水平也导致细胞生长迟缓与外膜异常,外膜蛋白组整体下调,与完全耗竭结果一致。
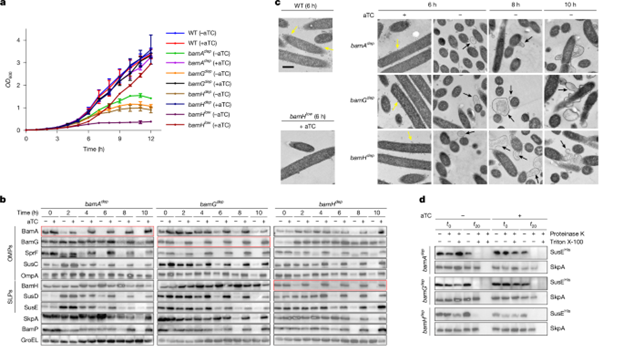
图3. BAMFj 必需亚基的耗竭分析
最后,为探究 BamG、BamH对 BAMFj 功能的作用,研究筛选到 BamH耗竭菌株的自发抑制突变体,其 BamA 存在Q801K 替换(即 BamHsup菌株)。该突变使菌株在缺失 BamH 及同源物BamH2 时,仍能像野生型一样正常生长(图 4a、b),且细胞形态、外膜完整性等表型正常(图 4c),SusCDE等蛋白水平与复合物组装也恢复正常,但 BamA Q801K 突变无法替代BamG,说明二者功能不同。外膜蛋白质组分析显示,多数OMP 和 SLP 水平恢复(图 4d),但部分SusCD 及其 SLP 伴侣对BamH 缺失敏感,提示 BamH 可能对特定SUS 系统的生物发生尤为重要。
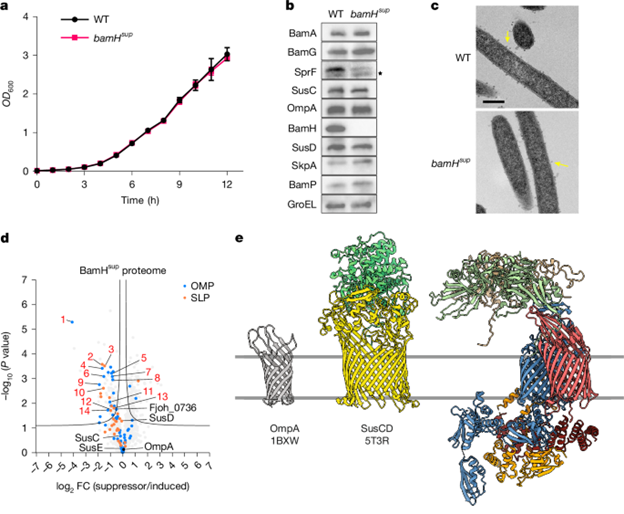
总结与亮点
研究发现Bacteroidota 的 BAM 复合体核心由 BamA、BamD、BamG、BamH 组成,并进化出独特“穹顶”结构以辅助大型外膜蛋白折叠。此外,BamH 对部分 SusCD 系统的组装至关重要,但 BamA Q801K 突变可弥补其缺失。说明 BamH 并非绝对必需,而是参与特定底物或错误折叠修复的质量控制过程。总体而言,Bacteroidota 的 BAM 复合体经过结构与功能上的重大改造,以适应其复杂外膜蛋白(如 SusCD 和 SLP)的生物发生需求,这种复杂 BAM外膜特性密切相关。









