2025.08.11~2025.08.17
CNS刊登文章
01
Nature
2025/08/13
1.“NASP modulates histone turnover to drive PARP inhibitor resistance”
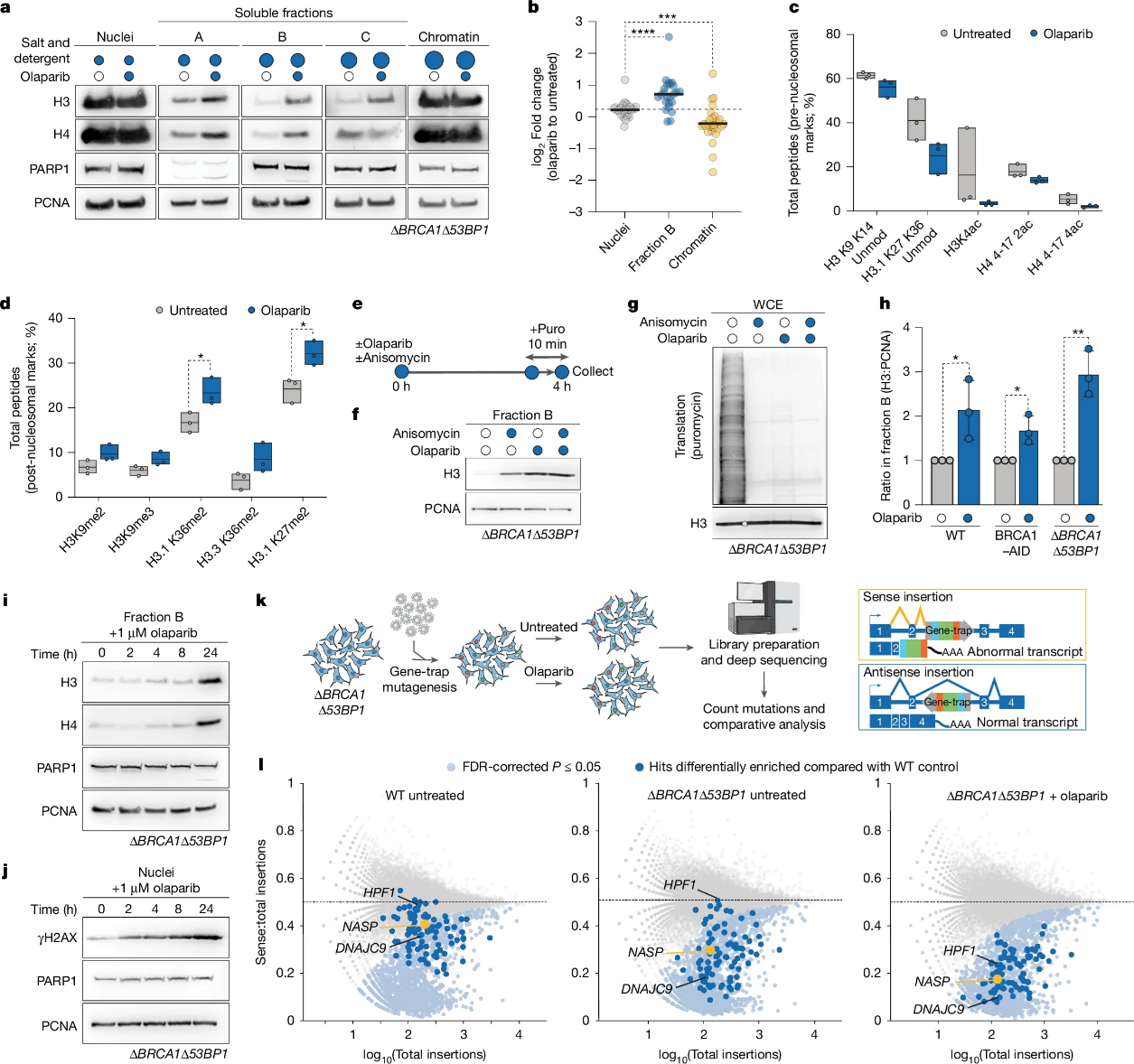
多聚(ADP-核糖)聚合酶抑制剂(PARPi)类药物代表了治疗同源重组缺陷肿瘤的一项重要进展,但耐药性仍然是一个挑战。尽管大多数研究集中在PARPi作用后的下游后果以应对耐药问题,但PARP抑制对染色质环境的直接影响及其对PARPi毒性的贡献仍不清楚。
来自荷兰Oncode研究所Jos Jonkers和Abdelghani Mazouzi课题组合作表明PARP抑制会诱导组蛋白从染色质中释放。这一现象揭示了PARPi耐药癌细胞的一个脆弱点:它们需要组蛋白稳态机制来维持较高的DNA复制速率和存活。通过功能性遗传学筛选,研究者发现NASP是维持被驱逐组蛋白稳定性的关键因子,其TPR结构域发挥作用。缺失NASP会使肿瘤细胞对PARPi治疗高度敏感,在体内外均会导致复制叉延伸受损及复制相关DNA损伤水平升高。此外,NASP与INO80复合物及PARP1的伴侣活性共同作用,以确保高效的组蛋白周转,防止致死性DNA损伤的累积。综上,本研究揭示了组蛋白驱逐是PARPi治疗的直接细胞响应,并为通过靶向组蛋白供应通路克服PARPi耐药提供了一条有前景的思路。
2025/08/13
2.“Expanding the cytokine receptor alphabet reprograms T cells into diverse states”

T细胞通过进化过程中形成的受体二聚体响应细胞因子,这些受体二聚体能够激活经典的JAK–STAT信号通路和基因表达程序。然而,JAK–STAT受体配对的潜在组合多样性可以通过探索非天然配对的未知生物学而得到扩展。
来自斯坦福大学医学院K. Christopher Garcia和Anusha Kalbasi课题组合作利用T细胞上作为共享信号枢纽的γ链(γc)受体,并通过一种正交的细胞因子受体平台,强制表达天然和非天然的异源二聚体JAK–STAT受体配对,从而扩展γc信号编码。 研究者测试了来自γc细胞因子的受体,以及干扰素、IL-10和本不与γc配对或在T细胞中自然不表达的同源二聚体受体家族。这些受体不仅能模拟它们的天然对应物,还能诱导情境特异性的转录程序。 这导致了肿瘤中T细胞的不同命运,包括由正交GCSFR(oGCSFR)驱动的具有吞噬能力的髓系样T细胞,以及由正交IL-4R(o4R)驱动的2型细胞毒性T细胞(TC2)和辅助性T细胞(TH2)分化。 表达正交IL-22R(o22R)和oGCSFR的T细胞——二者在T细胞中均非天然表达——表现出干细胞样和抗耗竭的转录及染色质特征,从而增强了抗肿瘤特性。 非天然受体配对及其产生的JAK–STAT信号为多样化T细胞状态开辟了新的路径,超越了天然细胞因子所能诱导的范围。
02
Science
本周无
03
Cell
2025/08/11
“NRT1.1B acts as an abscisic acid receptor in integrating compound environmental cues for plants”
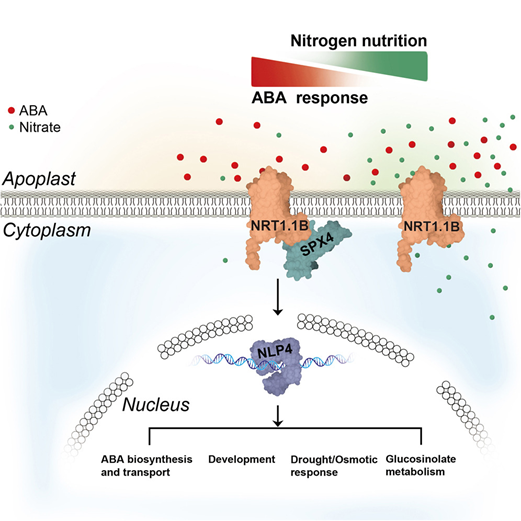
脱落酸(ABA)是植物适应环境条件的最关键植物激素。尽管植物中的 ABA 信号网络已被深入研究,但我们对多样化的 ABA 感知系统仍知之甚少。
华南农业大学胡斌和储成才以及南方科技大学龚欣团队合作发现高硝酸盐条件下,对 ABA 的转录响应受到抑制;而在低硝酸盐条件下,该响应显著增强,提示 ABA 信号与养分状态紧密整合。有趣的是,传统上被视为硝酸盐转运体与受体的 NRT1.1B 对 ABA 表现出显著更高的亲和力,并促成形成一个由 ABA 促进的 NRT1.1B–SPX4 复合物。该复合物触发释放被 SPX4 捕获的转录因子 NLP4,从而启动对 ABA 的转录响应。上述发现确立了 NRT1.1B 作为 ABA 受体的功能。值得注意的是,硝酸盐与 ABA 对 NRT1.1B 的竞争性结合揭示了一种机制,使 ABA 响应能够灵活适应波动的养分条件,展现出整合复合环境线索的精巧策略。
2025.08.11~2025.08.17
子刊刊登文章
01
Cell Research
8.15
“Constitutive arrestin recruitment by orphan GPR52 via an atypical binding mode”
02
Molecular Cell
本周无
03
Nature Structural & Molecular Biology
8.12
1.“Cytoplasmic PXR regulates glucose metabolism by binding mRNAs and modulating their stability”
04
Nature Communications
8.11
8.11
8.11
3.“Structural insights into Type II-D Cas9 and its robust cleavage activity”
8.11
4.“Molecular basis of human taurine transporter uptake and inhibition”
8.11
8.12
8.12
7.“Structural basis for membrane microdomain formation by a human Stomatin complex”
8.12
8.“Structure guided functional analysis of the S. cerevisiae Mre11 complex”
8.13
8.13
10.“The structure of the mammalian bornavirus polymerase complex”
8.13
8.14
8.15
13.“Structural basis for substrate recognition mechanism of human SLC26A7”
8.15
8.15
8.16
8.16
17.“Alpha-synuclein interacts with regulators of ATP homeostasis in mitochondria”
8.16
05
Science Advances
8.13
1.“Structures of MmpL complexes reveal the assembly and mechanism of this family of transporters”
8.15









