2025.08.18~2025.08.24
CNS刊登文章
01
Nature
2025/08/20
1. “Molecular mechanism of ultrafast transport by plasma membrane Ca2+-ATPases”
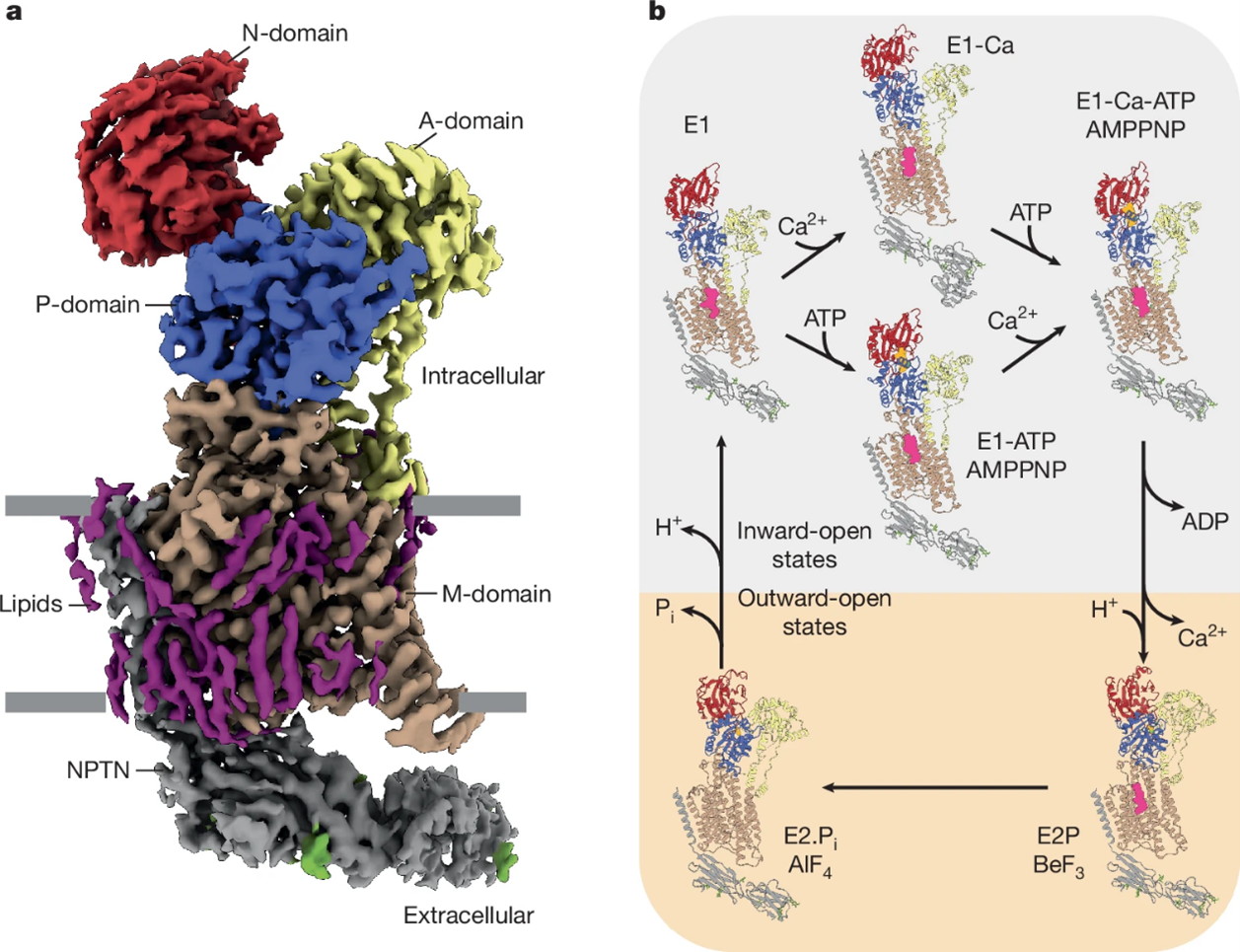
细胞内 Ca²⁺ 水平的严格控制 至关重要,因为 Ca²⁺ 被用来调控大量的信号转导途径。质膜钙泵(PMCA) 在这一过程中发挥关键作用,它们能够将 Ca²⁺ 逆浓度梯度从细胞质泵出到细胞外空间²。尽管关于 PMCA 生物学的新细节不断被揭示,但这些泵最显著特征的结构基础——即千赫兹量级的转运速率 以及 由质膜磷脂 PtdIns(4,5)P₂ 调控活性——迄今仍不清楚。
来自德国弗赖堡大学医学院生理学研究所的Bernd Fakler和Stefan Raunser合作报道了小鼠 PMCA2 在有无辅助亚基 neuroplastin 情况下,处于其转运循环八个不同阶段的结构。结合能够精确追踪完整细胞中 PMCA 介导的 Ca²⁺ 排出的全细胞记录,这些结构使研究者得以建立首个全面的 PMCA 转运模型,揭示致病突变的作用机制,并阐明了 PMCA–磷脂相互作用的结构基础。研究发现,PtdIns(4,5)P₂ 在转运循环依赖性的动态变化是其作为“闩锁”的根本所在:它促进 Ca²⁺ 的快速释放,并为对向离子的通过打开通道。这些作用对于维持超高速的转运循环是必需的。此外,研究者鉴定了 PtdIns(4,5)P₂ 结合位点,这一位点出乎意料地成为可通过药物操纵细胞内 Ca²⁺ 水平的潜在靶点。本研究为原生PMCA 型 Ca²⁺ 泵独特的快速运转机制 及其受膜脂和药物调控的分子机理提供了详细的结构学见解。
2025/08/20
2.“Structural basis for the dynamic regulation of mTORC1 by amino acids”
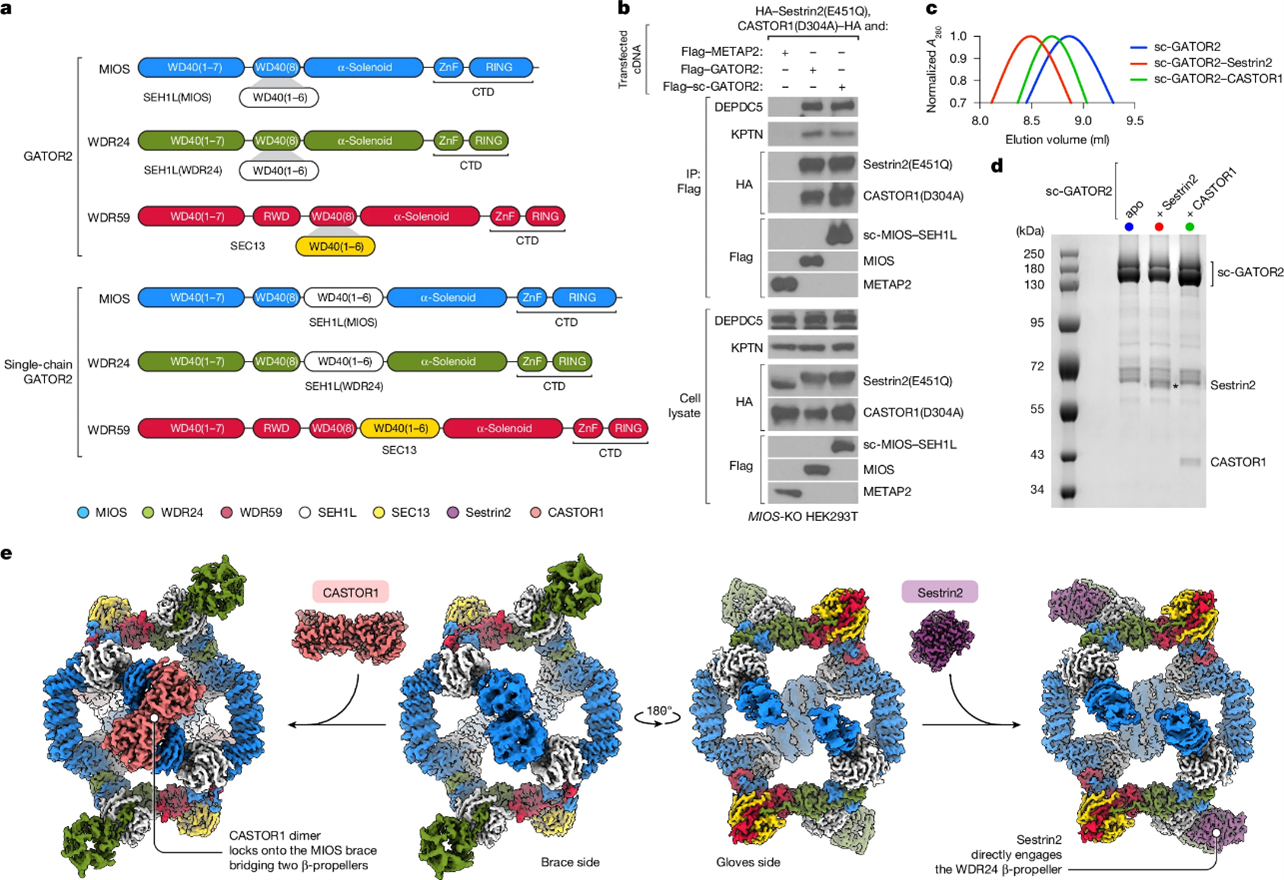
雷帕霉素靶蛋白复合物 1(mTORC1)是一个高度保守的信号通路的核心节点,它根据营养物质的可利用性调节细胞生长。氨基酸通过 Rag GTP 酶 激活 mTORC1,而 Rag GTP 酶又受 GATOR 调控。GATOR 是由 GATOR1、KICSTOR 以及营养感知核心 GATOR2 组成的超复合物。GATOR2 构成一个八边形笼状结构,其独特的 WD40 结构域 β-螺旋桨与 GATOR1、亮氨酸传感器 Sestrin1/2 (SESN1, SESN2) 以及精氨酸传感器 CASTOR1 相互作用。但这些传感器如何调控 GATOR2,以及它们在结合相应氨基酸后如何从 GATOR2 解离,目前仍不清楚。
来自美国斯坦福大学医学院Kacper B. Rogala和David M. Sabatini课题组合作利用冷冻电镜解析了与 Sestrin2 或 CASTOR1 结合的稳定化 GATOR2 结构。结果显示,这些传感器占据不同且不重叠的结合位点,一旦破坏这些位点,会选择性地削弱 mTORC1 感知特定氨基酸的能力。研究者还解析了 Sestrin2 的 apo(无亮氨酸)结构,并表征了 Sestrin2 和 CASTOR1 在氨基酸结合后发生的构象重排,这些变化触发了它们从 GATOR2 的解离。此外,任一传感器的结合都会限制 GATOR2 中 WDR24 β-螺旋桨的动态性,而该结构域对于营养依赖的 mTORC1 激活至关重要。这些发现揭示了氨基酸充足信号传递至 GATOR2 的别构机制,以及随之引发的结构变化如何导致 mTORC1 的激活。
02
Science
本周无
03
Cell
2025/08/18
1.“Conversion of IscB and Cas9 into RNA-guided RNA editors”
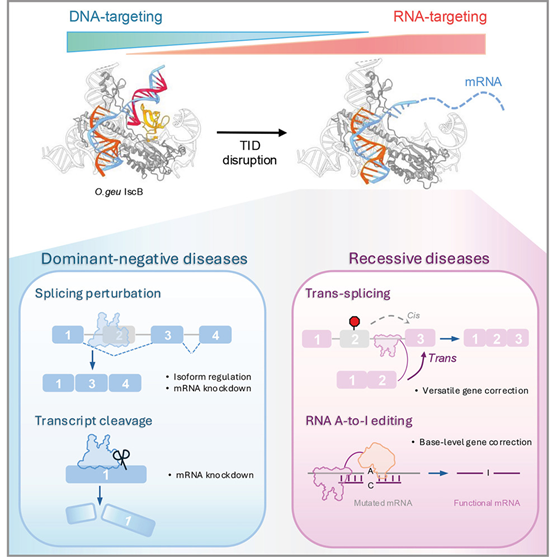
RNA 引导的 RNA 编辑为 DNA 编辑提供了一种有吸引力的替代方案。然而,目前主流工具 CRISPR-Cas13 存在伴随性的 RNA 切割活性,在人类细胞中会引发不良的细胞毒性。
来自耶鲁大学可爱龙课题组报道了一种基于 IscB 工程化改造的超紧凑型 RNA 编辑平台,其活性与 Cas13 相当或更高,但没有细胞毒性的担忧。研究者发现,作为 Cas9 的进化祖先,IscB 具有对互补的单链 DNA(ssDNA)和 RNA 的天然亲和力。当通过删除其 靶邻基序(target-adjacent motif, TAM) 结构域来关闭双链 DNA 的结合活性时,这种单链亲和活性会成为主要功能。所得的 R-IscB 在性能上可与 Cas13 相当甚至更优,能够在人体细胞中高效改变剪接结果,并且还能介导 转剪接(trans-splicing),在 mRNA 水平上校正任意突变。此外,当 R-IscB 与 RNA 腺苷脱氨酶 ADAR2 融合时,还可在 mRNA 上实现高效的 A-to-I 编辑;而在其 HNH 结构域上进行工程化改造后,则可介导基于切割的 mRNA 降解。最后,研究者进一步证明,该策略同样能够将某些 Cas9 转化为 RNA 靶向工具。
2025/08/18
研究提出一种肽调节剂的从头设计,以逆转与心律失常和癫痫相关的钠通道功能障碍
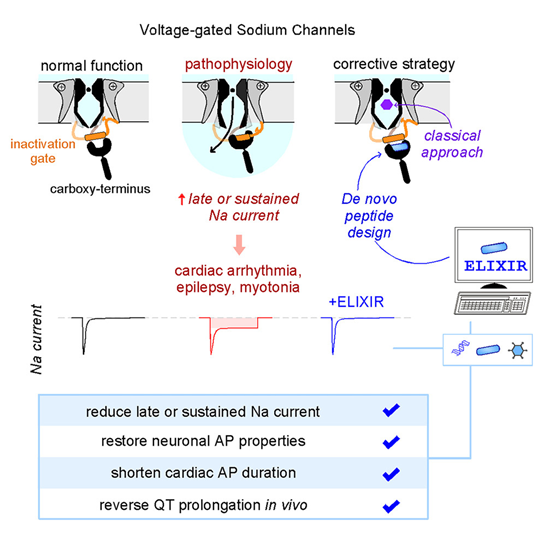
离子通道在可兴奋细胞中协调电信号的传导。在自然界中,离子通道的功能由调节蛋白加以定制,以满足不同的生理需求。然而,要人工设计出能够精确调控离子通道功能的合成调节因子仍然具有挑战性。一个典型例子是电压门控钠通道(NaV),它负责动作电位的起始;而当其功能异常时,会放大晚期/持续性钠电流(INaL)。这种病理性的电流增强是多种人类疾病(包括心律失常和癫痫)的共同机制。
来自哥伦比亚大学Manu Ben-Johny小组利用计算蛋白设计平台,创造了一种全新的肽类调节剂,命名为 ELIXIR(engineered late-current inhibitor X by inactivation-gate release)。它能以亚微摩尔亲和力结合 NaV 通道。功能分析显示,ELIXIR 在抑制“致病性” INaL 方面表现出意料之外的选择性,并在细胞和小鼠模型中有效逆转了与心律失常和癫痫相关的 NaV 功能异常。这些发现不仅证明了全新蛋白设计在合成离子通道调节剂上的有效性,也为未来理性设计治疗性新策略奠定了基础。
2025/08/18
“The small GTPase Ran defines nuclear pore complex asymmetry”
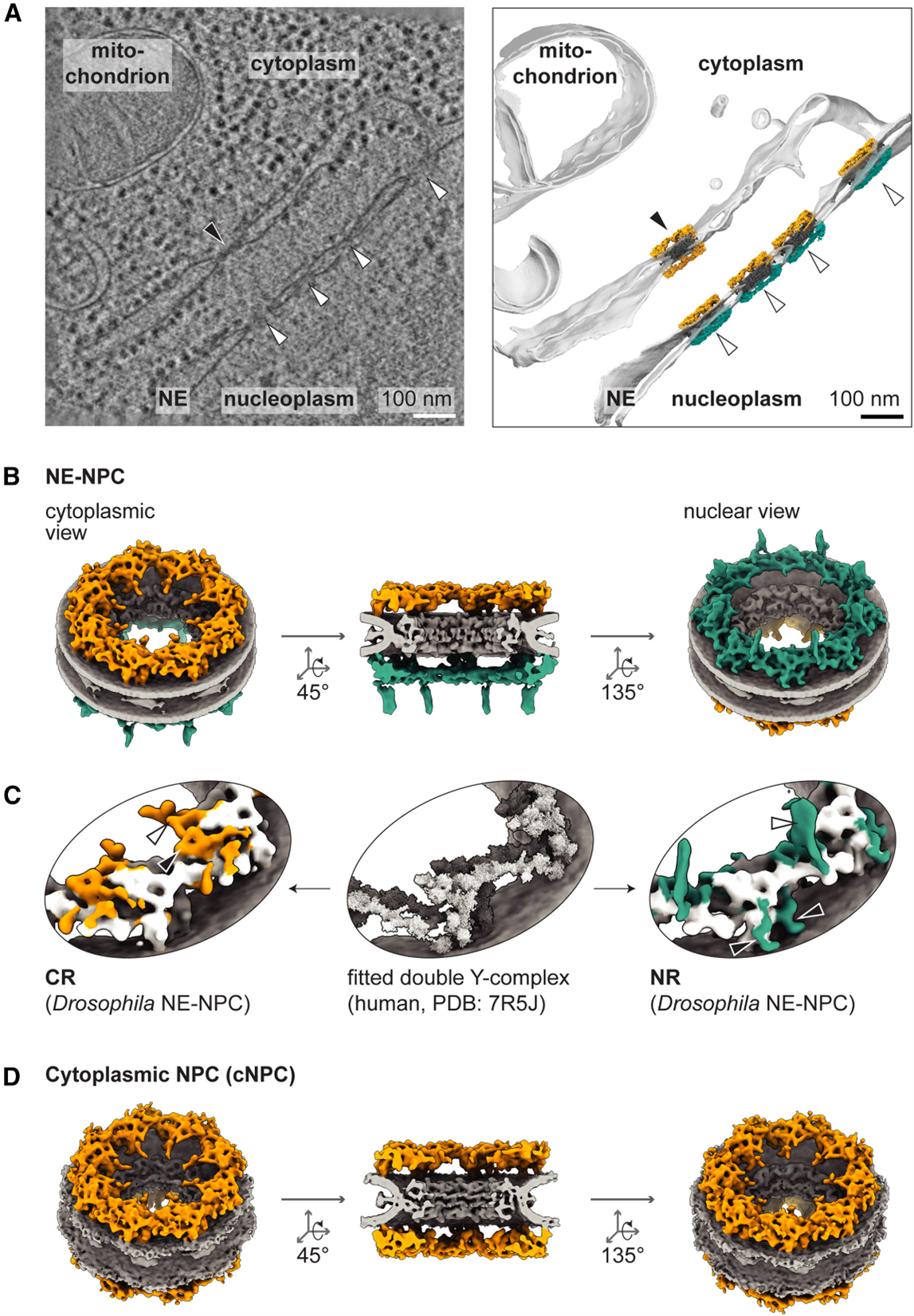
核孔复合物(NPCs) 横跨核膜,介导核质间的物质交换。它们由数百个核孔蛋白(nucleoporin)构成,是大分子组装体结构复杂性的典型代表。为了确保转运的方向性,不同的核孔蛋白复合物分别附着在 NPC 的细胞质面和核面。然而,这些不对称结构如何能够准确地组装到本身对称的支架结构上(该支架在两侧暴露出相同的相互作用界面),一直是个谜。
来自马克斯·普朗克生物物理研究所Bernhard Hampoelz和Martin Beck课题组合作结合了冷冻电子断层扫描、亚断层平均和模板匹配,并辅以活细胞成像,在酵母和果蝇中探讨这一问题。研究者通过遗传手段诱导形成异位核孔,并证明核膜之外的孔道呈对称性。进一步发现,小型 GTP 酶 Ran 的核苷酸状态会影响 NPC 外围结构的构型。这些发现表明,核转运系统是自我调控的——即相同的分子机制既控制转运过程,也控制转运通道的组装与组成。
2025.08.18~2025.08.24
子刊刊登文章
01
Cell Research
本周无
02
Molecular Cell
本周无
03
Nature Structural & Molecular Biology
8.18
8.22
04
Nature Communications
8.18
8.18
2.“Molecular basis of ligand binding and receptor activation at the human A3 adenosine receptor”
8.19
8.19
8.20
8.20
6.“IWS1 positions downstream DNA to globally stimulate Pol II elongation”
8.20
8.20
8.21
9.“Structures and mechanisms of U6 snRNA m6A modification by METTL16”
8.21
8.21
8.21
12.“Visualizing acyl carrier protein interactions within a crosslinked type I polyketide synthase”
8.22
8.23
8.23
8.23
16.“Structure-guided engineering of type I-F CASTs for targeted gene insertion in human cells”
8.23
8.24
18.“4D structural biology–quantitative dynamics in the eukaryotic RNA exosome complex”
05
Science Advances
8.22
1.“Characterization of the glycoproteins of fish and amphibian influenza B–like viruses”
8.22
2.“Mechanism and cellular actions of the potent AMPK inhibitor BAY-3827”
8.20
8.20
4.“Mechanistic insights into TTLL11 polyglutamylase–mediated primary tubulin chain elongation”









