提起钙,你想到的是什么?强健的骨骼、美味的牛奶?对于我们脊椎动物来说,身体里有一套精密的“调钙系统”——甲状旁腺激素(PTH),它就像一位严谨的仓库管理员,当血液中的钙不足时,就从骨骼这个“大仓库”里调取库存,确保生命活动正常运转。那么问题来了:那些没有骨头、甚至连PTH基因都找不到的昆虫,比如实验室里毫不起眼的果蝇,它们是怎么解决“缺钙”这个生存难题的呢?难道它们就不需要钙吗?当然不是!肌肉收缩、神经信号传递,这些生命核心活动都离不开钙离子。
2025年10月22日,日本筑波大学Naoki Okamoto和Ryusuke Niwa团队一项在顶级期刊《Nature》上发表了一篇题为“Neuroendocrine control of calcium mobilization in the fruit fly”的研究,为我们揭开了这个令人惊叹的生命奥秘。原来,果蝇体内藏着一套我们从未知晓的“内分泌调钙系统”,其精巧程度,堪称昆虫版的“人体甲状旁腺”!

确立钙缺乏的表型与内部钙库的存在
研究人员发现饮食钙缺乏会导致果蝇出现一系列的生理缺陷:幼虫活力大减,行动迟缓;肌肉收缩的力道和频率都大打折扣;最明显的是化身“长条怪”,它们化成的蛹变得又细又长,完全没了正常蛹圆润的体态(图1)。所以提示果蝇体内存在一个能缓冲饮食钙波动的内部钙动员系统。那么这个神秘的内部钙动员系统是什么?
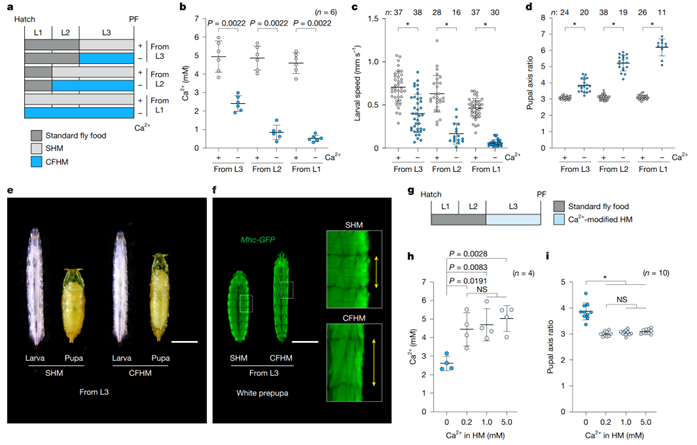
图1. 黑腹溞幼体发育过程中Ca2+缺乏的生理反应
基因“大搜捕”,锁定调控血钙的关键激素Capa
研究人员对51个神经肽基因进行RNAi筛选,发现敲低 Capa 基因会导致最显著的长蛹表型(图2)。而且发现Capa的mRNA特异性在中枢神经系统(CNS)中高表达,表明它可能作为一种神经内分泌因子发挥作用。然后通过通过表达谱分析和特异性染色,确定Capa由中枢神经系统的腹腹部神经元(VaNs)表达。特异性敲低VaN中的 Capa、或杀死/抑制VaN神经元,会重现长蛹和低血钙表型;激活VaN则能提升血钙。那么这就找到了“调钙司令部”(VaN神经元)和它发出的“指令”(Capa肽)。那么这个指令传递给谁呢?
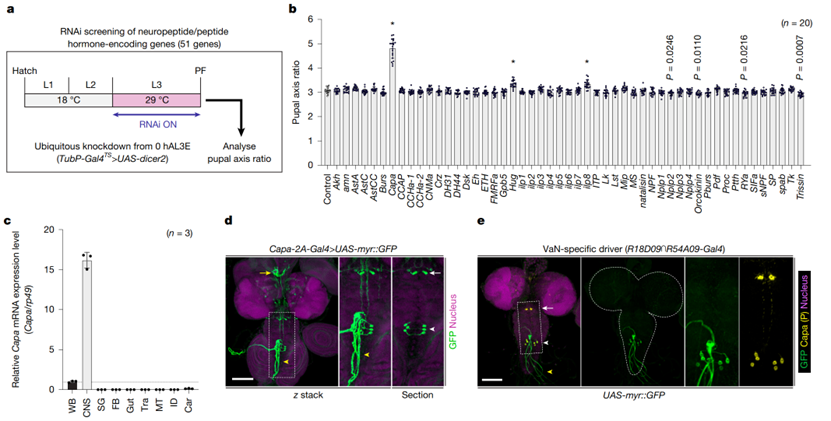
图2. 发现调控钙的神经内分泌因子Capa及其来源
之后表达谱分析和报告基因显示,Capa的受体CapaR在马氏管(Malpighian tubules)前段的初始区特异性高表达(图3)。
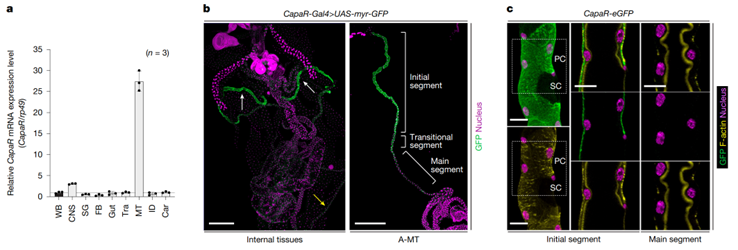
图3. Capa的受体 CapaR 在马氏管前段的初始区特异性高表达
马氏管作为钙库及Capa的动员机制
通过形态学观察、元素分析及定量检测,确证了马氏管前段起始段(IS)是一个特化的钙储存器官,其管腔内富含由钙磷化合物构成的珍珠样钙颗粒(PCGs),储存了机体近半的钙资源。关键的体外功能实验揭示,Capa神经肽(特别是Capa-1与Capa-2)能直接作用于离体的马氏管,通过其特异性受体CapaR,显著促进储存钙的释放。进一步地,研究者通过组织特异性基因敲降技术,在体内与体外层面均证明,CapaR的下游由Gαq蛋白(由CG17759编码)和蛋白激酶Cε(由Pkc98E编码)接力,共同构成了一条精确的信号转导通路,最终指令钙库“开闸”释放钙离子(图4)。
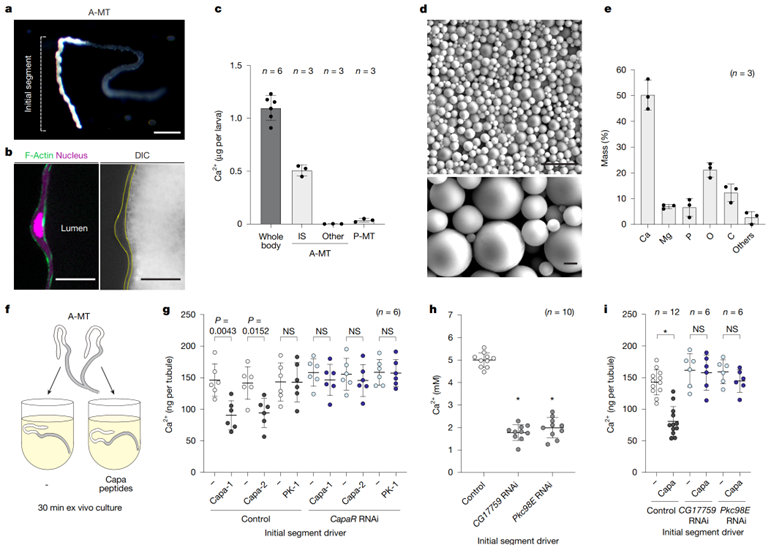
图4. Capa通过CapaR受体,激活Gαq-PKCε信号通路,动员马氏管钙库中的钙
之后研究人员将前面总结的分子机制置于整体的生理背景下,论证了Capa系统对于果蝇在真实世界中适应环境、维持生存的根本性重要性。研究证实,在饮食缺钙的危机下,该系统的激活对果蝇生存至关重要——野生型幼虫能通过动员马氏管钙库(PCGs减少)来缓冲危机,而CapaR突变体则因无法调用储备导致死亡率飙升。面对饮食钙波动,拥有完整Capa系统的个体能维持血钙稳定,而突变体的血钙水平则完全依赖食物供给,稳态失衡。最终,高钙饮食能特异性挽救突变体的所有表型,确凿证明了其一切生理异常的根源就是钙缺乏,从而完成了从分子机制到整体生理功能的完整因果论证。
总的来说,本研究首次在果蝇中揭示了一套完整的神经内分泌调钙轴。研究者发现,特定神经元(VaNs)分泌的Capa肽激素,作为关键信号,作用于马氏管起始段(IS)上的CapaR受体,通过Gαq-PKCε信号通路,动员其腔内的珍珠样钙颗粒(PCGs)释放钙离子至血淋巴。该系统对果蝇应对饮食钙缺乏、维持体内钙稳态及生存至关重要,其功能与脊椎动物的甲状旁腺激素(PTH)系统惊人地相似,展现了生命在演化中应对共同挑战的趋同策略。









